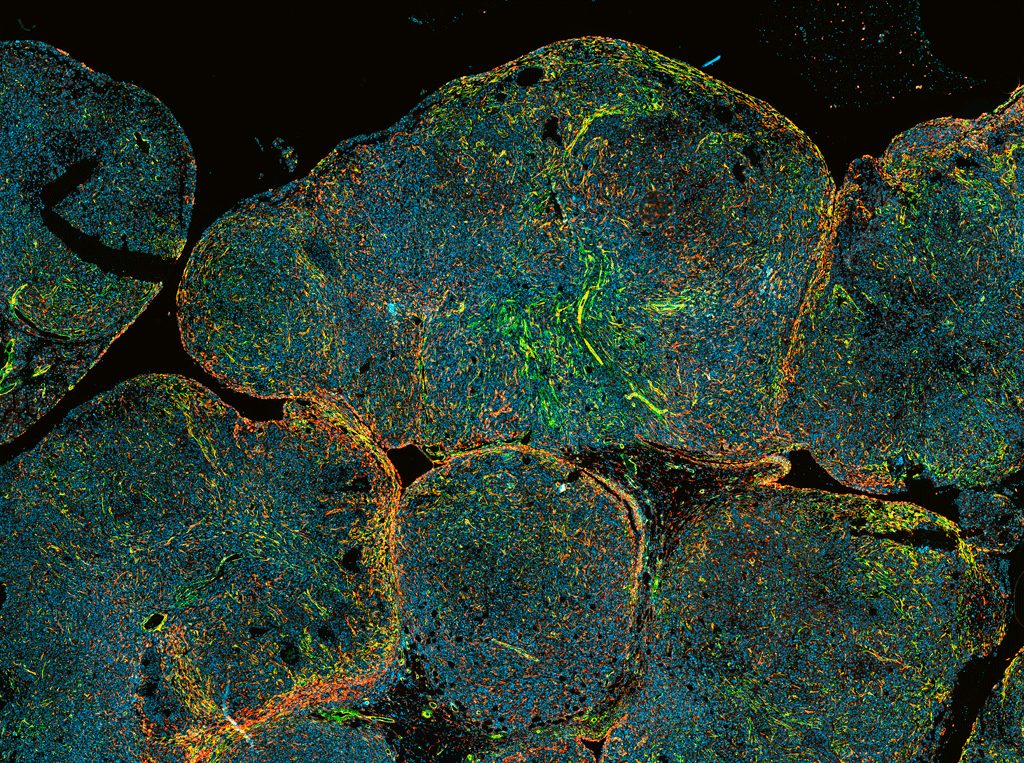
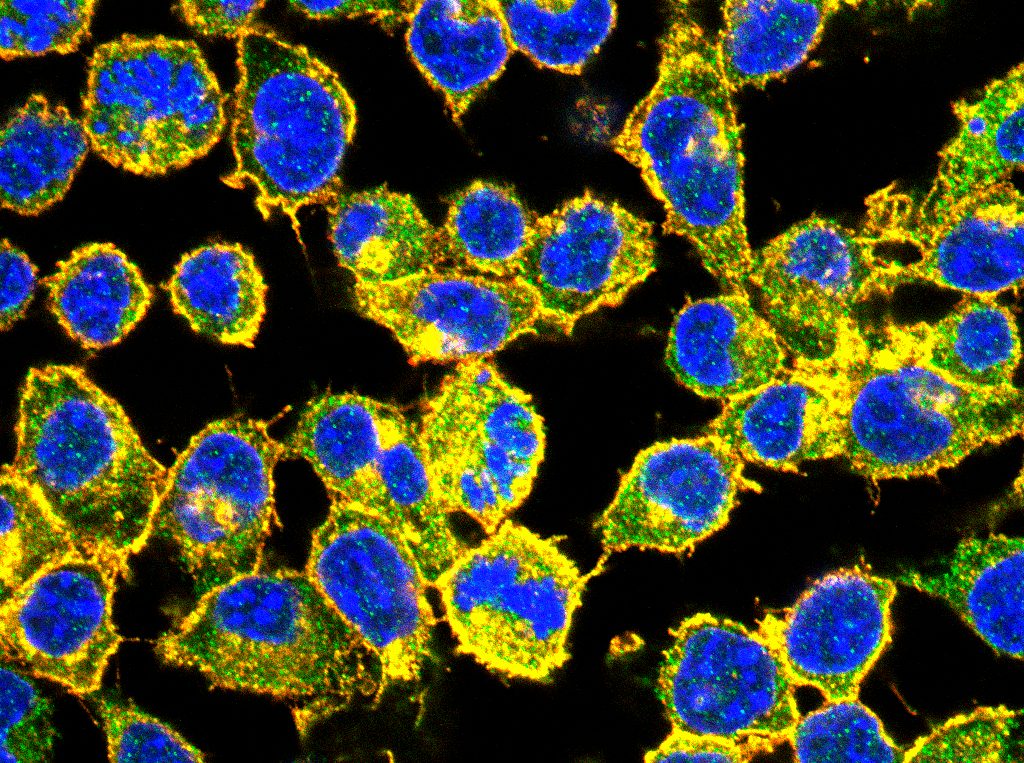
Estrategias para modular la conversación entre las células tumorales y su estroma.
A lo largo de mi carrera he trabajado con muchos tipos de células diferentes en distintos contextos. He trabajado con células musculares lisas vasculares en el contexto de la hipertensión y la aterosclerosis. He trabajado con macrófagos en el contexto de la biología tumoral. Y, por último, he trabajado con células endoteliales en el contexto de la disfunción endotelial y la biología tumoral. He contribuido a describir cómo las células tumorales alteran la composición de la membrana de los macrófagos, induciendo una desregulación en las vías de señalización que transducen la señalización inflamatoria, y que finalmente conducen a la supresión inmunitaria; también he contribuido a mostrar cómo las células tumorales inducen la senescencia de las células endoteliales, haciendo que el endotelio sea más permeable y potenciando la metástasis. Estos dos trabajos son la base de mi línea de investigación, que se centra en cómo las células tumorales y su estroma se comunican entre sí, y cómo esta interacción puede influir en el desarrollo del tumor. Aunque el grupo se centrará inicialmente en el cáncer de páncreas y de ovario, creemos que algunos de nuestros descubrimientos serían importantes para muchos otros tumores en los que el estroma es un importante motor de progresión. Emplearemos diferentes herramientas para modular la comunicación entre las células tumorales y su estroma con el fin de identificar posibles dianas terapéuticas y diseñar estrategias para regularlas.
Presentación
Conócenos mejor
Personal de investigación
El equipo que lo hace posible
Juan Rodriguez Vita
jrodriguez@cipf.es
Francesca De Angelis Rigotti
fangelis@cipf.es
Cristina Fandos Ramo
cfandos@cipf.es
Publicaciones
Nuestro aporte a la ciencia
Endothelial Notch1 signaling in white adipose tissue promotes cancer cachexia.
Taylor J, Uhl L, Moll I, Hasan SS, Wiedmann L, Morgenstern J, Giaimo BD, Friedrich T, Alsina-Sanchis E, De Angelis Rigotti F, Mülfarth R, Kaltenbach S, Schenk D, Nickel F, Fleming T, Sprinzak D, Mogler C, Korff T, Billeter AT, Müller-Stich BP, Berriel Diaz M, Borggrefe T, Herzig S, Rohm M, Rodriguez-Vita J and Fischer A
Nature Cancer, 2023 Nov, DOI: 10.1038/s43018-023-00622-y, Vol. 4, pag. 1544-1560
HAPLN1 potentiates peritoneal metastasis in pancreatic cancer.
Wiedmann L, De Angelis Rigotti F, Vaquero-Siguero N, Donato E, Espinet E, Moll I, Alsina-Sanchis E, Bohnenberger H, Fernandez-Florido E, Mülfarth R, Vacca M, Gerwing J, Conradi LC, Ströbel P, Trumpp A, Mogler C, Fischer A and Rodriguez-Vita J
Nature Communications, 2023 Apr, DOI: 10.1038/s41467-023-38064-w, Vol. 14, pag. 2353-2353
Semaphorin 3C exacerbates liver fibrosis.
De Angelis Rigotti F, Wiedmann L, Hubert MO, Vacca M, Hasan SS, Moll I, Carvajal S, Jiménez W, Starostecka M, Billeter AT, Müller-Stich B, Wolff G, Ekim-Üstünel B, Herzig S, Fandos-Ramo C, Krätzner R, Reich M, Keitel-Anselmino V, Heikenwälder M, Mogler C, Fischer A and Rodriguez-Vita J
HEPATOLOGY, 2023 Oct, DOI: 10.1097/HEP.0000000000000407, Vol. 78, pag. 1092-1105
Endothelial RBPJ is essential for the education of tumor-associated macrophages.
Alsina-Sanchis E, Mülfarth R, Moll I, Böhn S, Wiedmann L, Jordana-Urriza L, Ziegelbauer T, Zimmer E, Taylor J, De Angelis Rigotti F, Stögbauer A, Giaimo BD, Cerwenka A, Borggrefe T, Fischer A and Rodriguez-Vita J
CANCER RESEARCH, 2022 Dec, DOI: 10.1158/0008-5472.CAN-22-0076, Vol. 82, pag. 4414-4428
Membrane Cholesterol Efflux Drives Tumor-Associated Macrophage Reprogramming and Tumor Progression.
Goossens P, Rodriguez-Vita J, Etzerodt A, Masse M, Rastoin O, Gouirand V, Ulas T, Papantonopoulou O, Van Eck M, Auphan-Anezin N, Bebien M, Verthuy C, Vu Manh TP, Turner M, Dalod M, Schultze JL and Lawrence T
Cell Metabolism, 2019 Jun, DOI: 10.1016/j.cmet.2019.02.016, Vol. 29, pag. 1376
FONDOS
Gracias por apoyarnos